Pesquisar
FUVEST 1997 - 15973
O estudo cinético, em fase gasosa, da reação representada por NO2 + CO → CO2 + NO mostrou que a velocidade da reação não depende da concentração de CO2 mas depende da concentração de NO2 elevada ao quadrado. Esse resultado permite afirmar que a) o CO atua como catalisador. b) o CO é desnecessário para a conversão de NO2 em NO. c) o NO2 atua como catalisador. d) a reação deve ocorrer em mais de uma etapa. e) a velocidade da reação dobra se a concentração inicial de NO2 for duplicada.
UELONDRINA 1995 - 11208
No estudo cinético de uma reação representada por
2A(g) + B2 (g) → 2AB(g)
colocou-se os seguintes dados:
A velocidade da reação pode ser expressa pela reação
a) v = k 2[A]
b) v = k [B]2
c) v = k [A] [B]
d) v = k [A]2 [B]
e) V = K [A] [B]2
UFV 1996 - 11056
Para a reação CH3 Br + Cl- → CH3 Cl + Br as afirmativas a seguir estão corretas, EXCETO: a) aumentando-se a concentração de CH3 Br, aumenta-se a velocidade da reação. b) aumentando-se a concentração de Cl, aumenta-se a velocidade da reação. c) aumentando-se a temperatura, aumenta-se a velocidade da reação. d) aumentando-se as concentrações de Cl e CH3 Br, diminui-se a velocidade da reação. e) utilizando-se um catalisador, aumenta-se a velocidade da reação.
UFV 1996 - 11038
A formação do dióxido de carbono (CO2 ) pode ser representada pela equação C(s) + O2 (g) → CO2 (g). Se a velocidade de formação do CO2 for de 4mol/minuto, o consumo de oxigênio, em mol/minuto, será: a) 8 b) 16 c) 2 d) 12 e) 4
UFPE 1995 - 10654
A cinética da reação entre o óxido nítrico e o oxigênio, 2NO + O2 → 2 NO4 é compatível com o seguinte mecanismo: NO + O2 ↔ OONO (Equilíbrio rápido) NO + OONO → 2NO2 (reação aberta) A lei de velocidade para esta reação: ( ) É de primeira ordem em relação ao NO ( ) Não depende da concentração do intermediário OONO ( ) É de segunda ordem em relação ao NO2 ( ) É de segunda ordem em relação a ambos os reagentes ( ) Não apresenta constante de velocidade
PUCCAMP 1994 - 10516
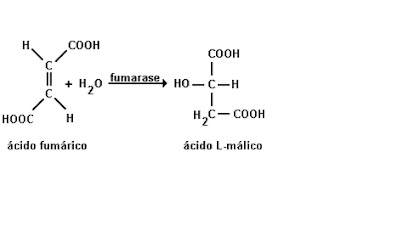
Numa das etapas do ciclo de Krebs ocorre a reação
Nessa reação a enzima fumarase atua como
a) oxidante; oxida o ácido fumárico.
b) redutor; reduz o ácido fumárico
c) ácido de Lewis; aceita par eletrônico oferecido pela água.
d) base de Lewis; fornece par eletrônico para a água.
e) catalisador; aumenta a velocidade da reação.
UFRJ 1996 - 10239
A oxidação do brometo de hidrogênio pode ser descrita em 3 etapas: I) HBr(g)+O2 (g)→ HOOBr(g) (etapa lenta) II) HBr(g)+HOOBr(g)→ 2 HOBr(g) (etapa rápida) III) HOBr(g)+HBr(g)→ Br2 (g)+H2 O(g) (etapa rápida) a) Apresente a expressão da velocidade da reação de oxidação do brometo de hidrogênio. b) Utilizando a equação global da oxidação do brometo de hidrogênio, determine o número de mols de Br2 produzido quando são consumidos 3,2g de O2. Dados: O = 16, Br = 80
MACK 1996 - 9913
Etapas: 1) HCOOH + H+ → (HCOOH2 )+ 2) (HCOOH2 )+ → (HCO)+ + H2 O 3) (HCO)+ → CO + H+ No mecanismo de decomposição do ácido metanóico, dado pelas etapas acima, o catalisador reage com um reagente numa etapa e é regenerado em outra. Então: a) o catalisador é o monóxido de carbono. b) a equação total é HCOOH ë (HCO)+ + H+. c) o ácido sulfúrico pode ser o catalisador. d) a fórmula do metanóico é (HCO)+. e) com o catalisador a reação é mais rápida, pois há um aumento da energia de ativação.
UECE 1996 - 9502
Seja a reação: X → Y + Z. A variação na concentração de X em função do tempo é:
A velocidade média da reação no intervalo de 2 a 5 minutos é:
a) 0,3 mol/L.min
b) 0,1 mol/L.min
c) 0,5 mol/L.min
d) 1,0 mol/L.min
UFC 1996 - 9312
Dado o diagrama de entalpia para os processos de adsorção e dissociação de O2 , em superfície de platina:
a) Calcule os valores das variações de entalpia, ΔH, para as seguintes etapas:
1) O2 (g) → O2 (adsorvido)
2) O2 (adsorvido) → 2 O (adsorvido)
3) O2 (g) → 2 O (adsorvido)
b) Calcule o valor da energia de ativação da etapa:
O2 (adsorvido ) → 2 O (adsorvido)
UFC 1996 - 9205
O óxido nítrico (NO), produzido pelo sistema de exaustão de jatos supersônicos, atua na destruição da camada de ozônio através de um mecanismo de duas etapas, a seguir representadas: (1) NO(g) + O3 (g) → NO2 (g) + O2 (g); ΔH= - 199,8 kJ (2) NO2 (g) + O(g) → NO(g) + O‚(g); ΔH = -192,1 kJ Assinale as alternativas corretas: 01. A reação total pode ser representada pela equação: O3 (g)+O(g) →2 O2 (g). 02. No processo total, o NO é um catalisador da reação. 04. Sendo V = k [O3][O] a expressão de velocidade para o processo total, a reação é dita de primeira ordem com relação ao ozônio. 08. Ambas as reações correspondentes às etapas do processo são endotérmicas. 16. A reação total fornecerá 391,1 kJ por mol de oxigênio formado. Soma ( )
UFPE 1995 - 8920
Você está cozinhando batatas e fazendo carne grelhada, tudo em fogo baixo, num fogão a gás. Se você passar as duas bocas do fogão para fogo alto, o que acontecerá com o tempo de preparo? a) Diminuirá para os dois alimentos b) Diminuirá para a carne e aumentará para as batatas c) Não será afetado d) Diminuirá para as batatas e não será afetado para a carne e) Diminuirá para a carne e permanecerá o mesmo para as batatas
UNAERP 1996 - 8810
A relação a seguir mostra a variação da concentração de uma substância A, em função do tempo em uma reação química:
aA + bB ↔ cC + dD
tempo / [A]
(min) / mol/L
0,0 / 11,0
2,0 / 7,0
4,0 / 4,3
6,0 / 3,0
8,0 / 2,0
10,0 / 1,0
12,0 / 0,5
14,0 / 0,3
16,0 / 0,2
18,0 / 0,2
Qual será o valor da velocidade média da reação de A correspondente ao intervalo entre 4 e14 minutos?
a) 4,0 mol.L-1 min-1
b) 0,40 mol.L-1 min -1
c) 1,4 mol.L-1 min-1
d) 25 mol.L-1 min-1
e) 2,5 mol.L-1 min-1
UFPE 1996 - 8763
Um determinado defensivo agrícola, quando exposto ao meio ambiente, decompõe-se através de uma reação química. Considerando que a velocidade de decomposição medida em laboratório apresentou os resultados a seguir:
Analise as afirmativas a seguir:
( ) A decomposição deste defensivo segue uma cinética de segunda ordem.
( ) O tempo para que a concentração do defensivo se reduza a valores desprezíveis independe da sua concentração inicial.
( ) A constante de decomposição do defensivo é de 0,02mês¢.
( ) O tempo de meia vida do defensivo é de [0,02/ln(2)] mês.
( ) A velocidade inicial de decomposição do defensivo é de 0,006g/l/mês para uma concentração inicial de 0,3g/l.
UNICAMP 1996 - 8285
O gráfico a seguir representa as variações das massas de um pequeno pedaço de ferro e de uma esponja de ferro (palha de aço usada em limpeza doméstica) expostos ao ar(mistura de nitrogênio, oxigênio, e outros gases além de vapor d'água).
a) Por que as massas da esponja e do pedaço de ferro aumentam com o tempo?
b) Qual das curvas diz respeito à esponja de ferro? Justifique.
PUCCAMP 1995 - 8272
Para diminuir a poluição atmosférica muitos carros utilizam conversores catalíticos que são dispositivos como "colméias" contendo catalisadores apropriados e por onde fluem os gases produzidos na combustão. Ocorrem reações complexas com transformações de substâncias tóxicas em não-tóxicas, como
Das seguintes afirmações acerca dessas reações
I. são todas de catálise heterogênea.
II. os catalisadores são consumidos nas reações.
III. os catalisadores aumentam a superfície de contato entre os reagentes.
IV. baixas temperaturas provavelmente aumentam a eficácia dos conversores catalíticos.
Pode-se afirmar que SOMENTE
a) I está correta
b) II está correta
c) III está correta
d) I e III estão corretas
e) II e IV estão corretas
UFPE 1996 - 8248
O gráfico a seguir representa a variação de concentração das espécies A, B e C com o tempo:
Qual das alternativas a seguir contém a equação química que melhor descreve a reação representada pelo gráfico?
a) 2A + B ë C
b) A ë 2B + C
c) B + 2C ë A
d) 2B + C ë A
e) B + C ë A
IME 1996 - 8204
Uma mistura gasosa ideal de propano e ar é queimada a pressão constante, gerando 720litros de CO2 por hora, medidos a 20°C. Sabe-se que o propano e o ar encontram-se em proporção estequiométrica. Determine a velocidade média de reação da mistura em relação ao ar, considerando a composição do ar 21% de O2 e 79% de N2 , em volume. Dados: Massas moleculares O = 16,00 N = 14,00
FEI 1995 - 8191
A combustão do butano (C4 H10) correspondente à equação: C4 H10 + (13/2)O2 → 4CO2 + 5H2 O + Energia Se a velocidade da reação for 0,05mols butano-minuto qual a massa de CO2 produzida em 01 hora? a) 880 g b) 264 g c) 8,8 g d) 528 g e) 132 g Massas atômicas: C = 12 u ; O = 16 u; H = 1 u
FATEC 1995 - 8142
Magnésio interage com ácidos segundo a equação:
Mg(s) + 2 H+ (aq) → Mg2+ (aq) + H2 (g)
Para o estudo dessa reação, duas experiências foram realizadas, tendo-se usado massas iguais de magnésio e volumes iguais de HCl 1mol/L e CH3 COOH 1mol/L. Os volumes de hidrogênio liberado foram medidos a cada 30s. Os resultados foram projetados em gráfico, como se mostra a seguir.
Das afirmações feitas sobre esse estudo, todas estão corretas, exceto uma. Assinale-a.
a) A rapidez de liberação de H‚ foi maior na exp. 1 do que na 2.
b) Na solução ácida usada na exp. 1 havia maior concentração de íons H+.
c) O ácido utilizado na exp. 1 foi CH3 COOH 1 mol/l.
d) Pode-se estimar que na exp. 1 todo o magnésio foi consumido ao fim de 55s, aproximadamente.
e) Pode-se estimar que, em ambas as experiências, o volume total de H‚ liberado foi 150cm3 , embora em tempos diferentes.
UFES 1996 - 8121
Para uma reação de 2ò ordem, em que a concentração é dada em mol/L e o tempo é dado em segundos, a unidade da constante de velocidade será a) s-1 b) mol . L-1 .s-1 c) mol-1 . L.s-1 d) mol-2 . L£.s-1 e) mol2 . L2 .s-1
CESGRANRIO 1994 - 8107
Cinco reservatórios de gás contém, respectivamente, os seguintes gases: I – CH4 II – C2 H2 III – C2 H6 IV – C3 H8 V – C4 H10 Em quais deles, por segurança, podemos aplicar um aumento de pressão suficiente para diminuir a velocidade de reação, caso ocorram nos reservatórios, reações de combustão, conforme se vê somente nas opções. a) I, II e III b) I, III e IV c) II, IV e V d) III, IV e V e) II, III e V
CESGRANRIO 1995 - 3820
Dado o diagrama de entalpia para a reação X+Y →Z a seguir, a energia de ativação para a reação inversa Z →X+Y é:
a) 60 kcal.
b) 35 kcal.
c) 25 kcal.
d) 10 kcal.
e) 0 kcal.
FUVEST 1996 - 3640
Em solução aquosa ocorre a transformação:
H 2O 2 + 2I + 2H+ → 2H2 O + I2
(Reagentes) (Produtos)
Em quatro experimentos, mediu-se o tempo decorrido para a formação de mesma concentração de I2 , tendo-se na mistura de reação as seguintes concentrações iniciais de reagentes:
Esses dados indicam que a velocidade da reação considerada depende apenas da concentração de:
a) H2 O2 e I.
b) H2 O2 e H+.
c) H2 O2 .
d) H+.
e) I.
VUNESP 1991 - 3233
O éter etílico pode ser obtido por aquecimento do álcool etílico, segundo a reação termodinamicamente possível: 2C2 H5 OH → C2 H5 -O-C2 H5 + H2 O Experimentalmente observa-se que o aquecimento direto do álcool puro não produz o éter esperado. Com a adição do ácido sulfúrico ao álcool etílico antes do aquecimento, ocorre a formação rápida do éter etílico. O ácido sulfúrico permanece quimicamente inalterado ao final da reação. Explique: a) Por que a reação de formação do éter etílico não ocorre na ausência do ácido sulfúrico, embora o processo seja energicamente favorecido? b) Qual o papel desempenhado pelo ácido sulfúrico na reação, que faz com que o processo ocorra rapidamente?
VUNESP 1991 - 3222
Uma mistura de dois volumes de H‚ gasoso e 1 volume de O‚ gasoso, quando submetida a uma faísca elétrica, reage explosivamente segundo a equação: 2H2 (g) + O2 (g) → 2 H2 O(g) liberando grande quantidade de energia. No entanto, se essa mistura for adequadamente isolada de influência externas (por exemplo, faísca elétrica, luz,...) pode ser mantida por longo tempo, sem que ocorra reação. Se, ao sistema isolado contendo a mistura gasosa, forem adicionadas raspas de platina metálica, a reação também se processará explosivamente e, no final, a platina adicionada permanecerá quimicamente inalterada. a) Explicar porque no sistema isolado, antes da adição da platina, não ocorre a reação de formação de água. b) Explicar porque a platina adicionada ao sistema isolado faz com que a reação se processe rapidamente.
UNICAMP 1991 - 3206
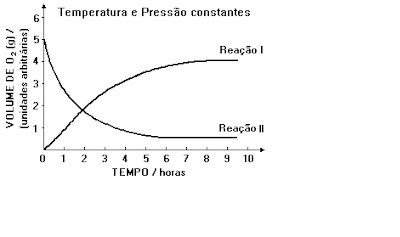
Numa reação que ocorre em solução (reação I), há o desprendimento de oxigênio e a sua velocidade pode ser medida pelo volume do O‚(g) desprendido. Uma outra reação (reação II) ocorre nas mesmas condições, porém consumindo O2 (g) e este consumo mede a velocidade desta reação. O gráfico representa os resultados referentes às duas reações:
Considerando as duas horas iniciais, qual das reações tem velocidade maior? Justifique sua resposta.
VUNESP 1992 - 3186
Se uma esponja de ferro metálico empregada em limpeza, como por exemplo o Bom Bril, for colocada em uma chama ao ar, inicia-se uma reação química. Esta reação prossegue espontaneamente, mesmo quando a esponja é retirada da chama, com desprendimento de material incandescente sob a forma de fagulhas luminosas. Após o término da reação, a esponja torna-se quebradiça e escura. No entanto, se um arame de ferro aquecido na mesma chama e também ao ar, a única alteração que se nota ao final é o escurecimento de sua superfície. a) Por que há grande diferença nas velocidades de reação nos dois casos? b) Escreva a equação balanceada da reação de formação de um possível produto da reação, com o respectivo nome, para os dois casos.
VUNESP 1992 - 3181
A oxidação do íon iodeto pelo peróxido de hidrogênio em meio ácido ocorre segundo a equação química balanceada: H2 O2 + 3I + 2H+ → 2H2 O + (I3 ) Medidas de velocidade de reação indicaram que o processo é de primeira ordem em relação à concentração de cada um dos reagentes. a) Escreva a equação de velocidade da reação. Como é chamada a constante introduzida nessa equação matemática? b) Os coeficientes da equação de velocidade da reação são diferentes dos coeficientes da equação química balanceada. Explique por quê.
FUVEST 1992 - 2827
A seqüência das reações I e II é proposta para explicar a destruição do ozônio da estratosfera. Os átomos de Cl se formam pela ação de radiação de alta energia sobre os clorofluorocarbonos(CFC).
a) Pode-se dizer que os átomos de cloro atuam como catalisadores na destruição do ozônio. Explique o porquê.
b) A destruição do ozônio representada pela equação III é favorecida por baixas ou altas temperaturas? Justifique com base no ΔH da reação.
VUNESP 1993 - 2766
Explique os seguintes fatos experimentais: a) Limalha de ferro dissolve-se mais rapidamente em ácido clorídrico se a mistura for submetida à agitação. b) A hidrólise alcalina de acetato de etila é mais rápida a 90°C de que a temperatura ambiente.
FUVEST 1993 - 2657
Para remover uma mancha de um prato de porcelana fez-se o seguinte: cobriu-se a mancha com meio copo de água fria, adicionaram-se algumas gotas de vinagre e deixou-se por uma noite. No dia seguinte a mancha havia clareado levemente. Usando apenas água e vinagre, sugira duas alterações no procedimento, de tal modo que a remoção da mancha possa ocorrer em menor tempo. Justifique cada uma das alterações propostas.
FUVEST 1993 - 2656
Hidrogênio reage com quase todos os elementos. Sua reação com nitrogênio produz amônia (NH3 ). Industrialmente essa reação é realizada na presença de um catalisador. a) Explique para que serve o catalisador. b) Calcule a porcentagem em massa de hidrogênio na amônia. Massas molares H = 1,0 g/mol N = 14,0 g/mol
UNITAU 1995 - 2141
Na reação de dissociação térmica do HI(g), a velocidade de reação é proporcional ao quadrado da concentração molar do HI. Se triplicarmos a concentração do HI, a velocidade da reação: a) aumentará 6 vezes. b) aumentará 9 vezes. c) diminuirá 6 vezes. d) diminuirá 9 vezes. e) diminuirá 3 vezes
UNITAU 1995 - 2082
Seja a reação de decomposição: 2N2 O5 → 4NO2 + O2 . Podemos afirmar que: a) a velocidade da reação pode ser calculada pela expressão v=k[N2 O5 ]2. b) a velocidade da reação pode ser calculada na forma: v=k[NO2 ]4.[O2 ].[N2 O5 ]2. c) a ordem global da reação é 5. d) é uma reação endotérmica, por causa do O2 . e) é uma reação exotérmica, por causa do NO2 .
UNICAMP 1995 - 1244
Soluções aquosas de água oxigenada, H2 O2 , decompõem-se dando água e gás oxigênio. A figura a seguir representa a decomposição de três soluções de água oxigenada em função do tempo, sendo que uma delas foi catalisada por óxido de ferro (III), Fe2 O3 .
a) Qual das curvas representa a reação mais lenta? Justifique em função do gráfico.
b) Qual das curvas representa a reação catalisada? Justifique em função do gráfico.
UNICAMP 1995 - 1239
O alumínio é um dos metais que reagem facilmente com íons H+ , em solução aquosa, liberando o gás hidrogênio. Soluções em separado, dos três ácidos a seguir, de concentração 0,1mol L¢, foram colocadas para reagir com amostras de alumínio, de mesma massa e formato, conforme o esquema adiante:
ÁCIDOS:
Ácido acético, Ka = 2×10-5
Ácido clorídrico, Ka = muito grande
Ácido monocloro acético, Ka = 1,4×10-3
a) Em qual das soluções a reação é mais rápida? Justifique.
b) Segundo o esquema, como se pode perceber que uma reação é mais rápida do que outra?
VUNESP 1995 - 1009
Em duas condições distintas, a decomposição do NH4 NO3 , por aquecimento, conduz a diferentes produtos: I. NH4 NO3 puro aquecimento NH4 NO3 (s) → N2 O(g)+2H2 O(g)+169kJ II. NH4 NO3 em presença de impurezas de cloreto: aquecimento NH4 NO3 (s) → N2 (g)+2H2 O(g)+1/2O‚(g)+273kJ Explique, em termos de energia de ativação: a) Por que a decomposição do NH 4NO3 puro ocorre pelo processo representado em I, embora aquele representado em II corresponda a um processo mais exotérmico. b) O papel do íon cloreto na decomposição representada em II.
FUVEST 1995 - 709
A reação de persulfato com iodeto
S2 O82- + 2I- → 2SO4 2- + I2
pode ser acompanhada pelo aparecimento da cor do iodo. Se no início da reação persulfato e iodeto estiverem em proporção estequiométrica (1:2), as concentrações de persulfato e de iodeto, em função do tempo de reação, serão representadas pelo gráfico:
linha grossa: concentração de I
linha fina: concentração de S2 O2-8
Na alternativa (c) as duas linhas coincidem.
FUVEST 1994 - 96
A obtenção de SO3 (g) pode ser representada pela seguinte equação: SO2 (g) +1/2 O2 (g) + catalisador ↔ SO3 (g) A formação do SO3 (g), por ser exotérmica, é favorecida a baixas temperaturas (temperatura ambiente). Entretanto, na prática, a obtenção do SO3 (g), a partir do SO2 (g) e O2 (g), é realizada a altas temperaturas (420°C). Justifique essa aparente contradição.
FUVEST 1994 - 39
NaHS4 + CH3 COONa → CH3 COOH+Na2 SO4 A reação representada pela equação acima é realizada segundo dois procedimentos: I. Triturando reagentes sólidos. II. Misturando soluções aquosas concentradas dos reagentes. Utilizando mesma quantidade de NaHSO4 e mesma quantidade de CH3 COONa nesses procedimentos, à mesma temperatura, a formação do ácido acético: a) é mais rápida em II porque em solução a frequência de colisões entre os reagentes é maior. b) é mais rápida em I porque no estado sólido a concentração dos reagentes é maior. c) ocorre em I e II com igual velocidade porque os reagentes são os mesmos. d) é mais rápida em I porque o ácido acético é liberado na forma de vapor. e) é mais rápida em II porque o ácido acético se dissolve na água.